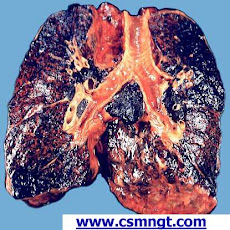
フラグミンはカルシウム依存下にアクチンと結合し、(アクチン線維の片端=barbed end に結合して) アクチンの重合を制御する "キャッピング蛋白" として機能するが、AF複合体中のアクチンがいったん燐酸化されると、キャッピング機能自体もカルシウム依存性になる。 しかも、カルシウム存在下では、AF複合体中のアクチンは燐酸化されない。 従って、(AF kinase は ) 非常に魅力ある酵素だった。
NIHで土壌アメーバからミオシンを燐酸化する「PAK」というキナーゼを見つけて以来、私はいわゆる「キナーゼの猟人」になっていた。当時、発癌キナーゼである「SRC」が発見され、新しいキナーゼを発見することが、若い生化学たちの間でブームになっていた。アクチンを燐酸化するキナーゼは誰も未だ見つけていなかった。 そこで、「AF kinase」は、その先駆となった。 ところが、一つ困ったことが生じた。 「PAK」は哺乳類にも存在するから、研究に「普遍性」があった。 ところが、「AF kinase」は、アメーバ以外では、その存在を証明し難かった。 従って、研究自体はすこぶる面白くとも、普遍性に欠ける可能性があった。
そこで、色々思案した結果、「Nature」誌に論文を発表後、「AF kinase」の研究を断念した。ギア=チェンジ (Recombinant DNA Technology の習得) をして、豪州に永住し、発癌の研究を開始してから間もなく、幸い「PAK」が発癌キナーゼであることが判明した。 こうして、我々の「PAK遮断剤の開発」研究が開始された。
他方、「AF kinase」については、発見から何と20年も経ってから、米国のインディアナ州立大学の研究グループによって、哺乳類細胞にも存在することが実証された。細胞をフォスファターゼ (脱燐酸化酵素) 阻害剤 (Calyculin A) で処理すると、アクチンの燐酸化が容易に検出されるようになった (1)。 更に、アクチンの燐酸化が細胞の癌化現象に関与している可能性も示唆されている (1, 2)。 従って、「AF kinase」もPAKと同様、発癌キナーゼである可能性がある。 更に、面白いことには、PAKは抗生物質「スタウロスポーリン」(ST)によって阻害されるが、アクチンの燐酸化はSTによって、阻害されない。
従って、今や「アクチンの燐酸化酵素 (キナーゼ) 」研究には十分に「普遍性」がある上、研究をしているグループがまだごく少ないので、「穴場」である。
なお、国立癌センターの研究によれば、「カリクリンA 」(Calyculin A) は海綿由来の燐酸化合物で、発癌作用があると共に、「カルシウムチャネル=ブロッカー」でもある (2)。
1980年代の後半まで、NIH/NCIに角永武夫という年配(50前後) の癌学者 (1988年に癌で他界) が活躍していた。 彼は癌細胞の中に不思議な beta-アクチンの変異体を見つけた。244番目のGLY がASPに置換されているミュータントである (3)。 このミュータントを正常な細胞に挿入すると、何故か癌化した。 しかしながら、そのメカニズムは不明のままに終わった。
さて、アクチンが燐酸化されると、201-203番目にあるTHRが特異的に燐酸化される。 通常、燐酸化されるアミノ酸を「酸性のアミノ酸」 (GLU かASP) に置換すると、燐酸化された場合と同様な挙動を蛋白が示す。
201-203 はアクチンの重合に関与している部分の一部 (pointed end) で、燐酸化が起こると重合し難くなる。 従って、201-203 番目付近にあるアミノ酸を「酸性のアミノ酸」で置換すると、重合し難くなるはずである。
さて、244番目がASPに置換された(アクチン) ミュータントも重合し難い (3)。 従って、これはまだ私の「想像の域」を脱しないが、201-203番目を「酸性のアミノ酸」に置換したミュータントを、正常細胞に挿入 (発現) すれば癌化する可能性がある。 もし、それが実証されれば、(PAKと同様) 「アクチン=キナーゼ」は発癌キナーゼということになる。 そうすれば、このキナーゼの阻害剤を開発すれば、癌を治療しうるはずである。
実際にアクチンの3次元 (立体) 構造を調べてみると、244番目と201-203 番目のアミノ酸は殆んど隣同志にある。 従って、私の想像は "9分通り" 的中している!
更に一歩進めて、PAK と(発癌キナーゼ候補である) 「アクチン=キナーゼ」(AK)との関係を探る目的で、水平思考を重ねてみよう。 PAK は「LIM kinase」を介して、「コフィリン」 と呼ばれる (フラグミン類似の機能を持つ) アクチン結合蛋白を燐酸化して、アクチンの重合を促進する。 従って、PAK が何らかの経路でAKを活性化して、アクチンの重合を促進する可能性もある。 それを実験的に確認するのはごく簡単にできる。
例えば、先ず癌細胞 (A549) を「カリクリンA 」で処理して、アクチンの燐酸化を確かめた後、更にPAK遮断剤でも細胞を処理して、アクチンの燐酸化が抑えられるかどうかを調べる。 もし、アクチン燐酸化が抑えられれば、AK (発癌キナーゼ) の活性化にはPAKが必須であることが実証される。。。 これに関連して、2001年にハーバード大学医学部の研究グループ (John Badwey ら) から、大変面白い報告が出ている。 好中球 (白血球の一種) を「カリクリンA 」で処理すると、PAKが活性化する(4)。 "エベレスト登頂" にたとえれば、我々(「PAKーAK」遠征隊) はようやく 「サウス=コル」付近にさしかかっている。最後の難所は「ヒラリー=チムニー (ステップ)」 と呼ばれる岩場である。 これを無事クリアできれば、"未踏の頂上" はすぐ間近である。
AKの発見は実は偶然だった。細胞性粘菌 (アメーバの一種) に存在するPAK以外のミオシン=キナーゼの活性がカルシウムによって阻害されることを発見してから、同じようなキナーゼが別の粘菌アメーバにも存在するかどうかを確かめている中に、フィザルムの場合は意外にも、アクチン=キナーゼがカルシウムによって阻害されることを見つけた。 そこで、私は研究テーマを「ミオシン=キナーゼ」から「アクチン=キナーゼ」へ変更した。 勿論、"細胞性粘菌"専門の教授は、テーマの変更に同意しなかったので、私は隣の"フィザルム"の研究室へ移動を決意した。 日本の大学や研究所では、このような「離れ業」はとてもできない。
参考文献:
1. Gu L,
Zhang H,
Chen Q,
Chen J.
Calyculin
A-induced actin phosphorylation and depolymerization in renal epithelial cells.
Cell Motil Cytoskeleton.
2003; 54(4):286-95.
2. Suganuma M, Fujiki H, Furuya-Suguri H, Yoshizawa S, Yasumoto S, Kato Y, Fusetani N, Sugimura T. (1990). Calyculin A, an inhibitor of protein phosphatases, a potent tumor promoter on CD-1 mouse skin。 Cancer Res. 50 (12): 3521-5.
3. Taniguchi S1, Sagara J, Kakunaga T. Deficient polymerization in vitro of a point-mutated beta-actin expressed in a transformed human fibroblast cell line. J Biochem. 1988. 103(4):707-13.
2. Suganuma M, Fujiki H, Furuya-Suguri H, Yoshizawa S, Yasumoto S, Kato Y, Fusetani N, Sugimura T. (1990). Calyculin A, an inhibitor of protein phosphatases, a potent tumor promoter on CD-1 mouse skin。 Cancer Res. 50 (12): 3521-5.
3. Taniguchi S1, Sagara J, Kakunaga T. Deficient polymerization in vitro of a point-mutated beta-actin expressed in a transformed human fibroblast cell line. J Biochem. 1988. 103(4):707-13.
4. Lian JP,
Toker A,
Badwey JA.
Phosphorylation
of the activation loop of gamma p21-activated kinase (gamma-Pak) and related
kinases (MSTs) in normal and stressed neutrophils. J Immunol. 2001; 166(10):6349-57.










































































![リオ五輪男子体操団体:日本(金)、ロシア[銀]、中国[銅]。](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEjHS61FORcH43CteZVfJzLmbqvNwOIliOSMpTpRtEi7x8j1ZwPk5rDaZovTrwuZxfDDtdEDSj673it735LF0mweIunaj7ja07lURBDYTV6wPMaAlumFt3aWWzYbHZgIaxcOLk_OKEMyQ3lX/s1600/2016+taiso+gold.jpg)
![皇太子(明仁)による沖縄訪問 [1975年]](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEjvSQrzV7yw_4gVQSwxZP_jh4VnEJscSqOqbiBh0VdAK3CRddXRqkd70JdLyws9fGejk-FGVmXWbHvSxlF3f8UogTyf9KXbqU1NGXesvcx2Hlsd6uq81AHweeioc61wynq3d2IYuyolijgT/s1600/akihito+message.jpg)

























































































































































































![アルニカ [ウサギ菊]](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEilqv0qou-4NpoUh1PFWYK0FSaozKazee0VYGxsFtfjBma46ya9yxqB6X9Ziuob25tNRpBbnFIcUFlOEjz1WcAjVNzjGl1E-QbDgE7VOLkjZDx0eplJ1WJHf0fTEWXxf8F5G-cHUhqHELY9/s1600/ArnicaS.jpg)








































































































































.jpg)


















































































.jpg)